���F�ڵ�λ�ã� �ٝ�����ˎ���W��� >> �[���� >> �[����Ҏ��ˎ�����
�ί�θ���ďͷ���ˎ�漪�W�z��(S-1)���о��Mչ
- ��Դ�� �����t�Wˎ�W�փ� ���ߣ������� �g�[�� �l���r�g��2009/11/20 8:30:00
���Ї���θ���İl���ʺͲ����ʾ��Ӑ����[������λ��Ŀǰ���R����θ�����\�Π�r���F���ߣ��l���ʸߡ��D���ʸߡ������ʸߣ������ͣ����\�ʵ͡��г��ʵ͡�5�������ʵͣ��ĬF����ˣ��о�θ��ȫ�������ɞ鮔ǰ�t�W����Ҫ���о�����
�漪�W�z�ң�S-1������ӷ���tegafur��FT�����W��1-���Ě�-2-ૻ�)-5-��-2��4��1 H��3 H)-��श�ͪ������ʽ��C8H9FN2O3�����������|����Mr��200. 17��������������gimeracil��CDHP�����W��5-��-2��4-���u����ण�����ʽ��C5H4C1NO2��Mr 145. 55���͊W������⛣�oteracilpotassium��OXO�����W��1��2��3��4-�Ě�-2��4-����-1��3��5-���-6-������}������ʽ��C4H2KN3O4��Mr195. 18���ďͷ��Ƅ����M��Ħ���Ȟ�1��0.4��1��ÿ���漪�W�z�ң�S-1�� �z���к�FT 20 mg��OXO 19. 6 mg��CDHP 5. 8 mg�����M�ֻ��W�Y��ʽҊ�D1��ԓˎ���ձ�̫��ˎ�I��˾�ׄ��_�l��1999�����ձ��״����У���Ʒ�����漪�W�z�ң�S-1��������Ҫ�m���C��θ�����^�i������Ŀǰ���漪�W�z�ң�S-1�����ձ��ѳɞ��ί�����θ�c�������[����һ��ˎ����겻�H���ɇ���ɽ�|�r��ˎ�I��˾���a���漪�W�z�ң���Ʒ�����S���_�������N�ۣ������ڽ����°����ձ����iˎ�I���a���漪�W�z�ң���Ʒ������˹�f��Ҳ�ѽ����Ї����С�
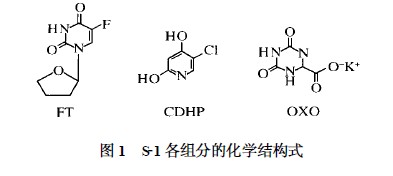
1 ˎ���Ͷ���W
1. 1 �M������
�漪�W�z�ң�S-1����FT��CDHP��OXO ��1��0. 4��1 ��Ħ���ȽM�ɵďͷ��Ƅ�������FT ��5-������ण�5-FU����������ڷ����ս����K���w�ļ���ɫ��P-450 øϵ�y�����D����5-FU�l�]�������á�5-FU��Ŀǰ������V��������ˎ����������[�����������w�������õį�Ч�����[��������ռ����Ҫ��λ��FT �������c5-FU��ͬ�����w���ܸɔ_�����DNA��RNA�������|�ĺϳɡ�����������䶾��ֻ��5-FU��1/ 7��1/ 4������ָ����5-FU��2�������Զ��Ԍ����δҊ���صĹ������ƣ�������ϵ�y��Ӱ����^�p����ԭ������FT�γ�5-FU�ֽ���x�a��Ŀ����Ժ�С���Ķ����p����5-FU�ֽ���x�a��Ķ��ԡ�
FT�Ļ��Դ��x�a��5-FU���w�ȘO���������ױ��������ٺ��[���M���a���Ķ������Ó��ø��DPD�����ٽ��⣨�_85 %���ϣ���ʧ������M�����[���M���е�DPD �����cDPD mRNA ���������^���@�Ă��w����Ķ����FT �Ŀڷ��������ö�׃�������ܴ���0 %��77 % �ķ����Ȳ��ӡ��@�������������ˎ��ˎЧ�����Ҫԭ��ֱ������DPD ���ܕ��p���@�N������ƌ�����������еęC�w�M����θ�c�ں����е�DPD���ܜp�ٷ�����स���������Ą������w��������[���M���е�DPD�������L��������ˎ������Õr�g�����ң����[���M���е�DPD�������ӣ���5-FU�Ľ����������ӣ��Ķ��@����ˎ�ԕr��Ҳ��ͨ�^����DPD��������ˎ�ԡ�CDHP��һ�NDPD ���Ƅ������w������DPD �����Ƿ�����व�180�����ɜp��5-FU�ķֽ��ٶȣ����Lˎ���Ч�r�g���p�ق��wˎЧ���
FT�����ữ���x�a��——�������-����Ó�����գ�FdUMP������Ҫ�Ŀ����ɷ֣���Ҳ��FT���lθ�c���������õ���Ҫ���|��OXO�ڷ����պ����θ�c���x���Ե�������������������ǻ��D��ø�������5-FU���ữ���p�p��FT�����θ�c�������á�ԇ�Y������������OXO���@������FT ���l�ĸ��a��ʳ���p�˵�θ�c�������á�
1. 2 ˎ�������W
OXO�ڷ����պ���Ҫ�ֲ���С�c��������FT�Ļ��Ԯa��5-FU���ữ���Ķ��p�pFT ��θ�c���a���ļ��������á�OXO�������M���зֲ����٣���˲����ɔ_FT�Ŀ��[�����á�OXO�Ĵ��x;����Ҫ�Ѓɗl����OXO���c����Ⱥ���������D����K�a���������ᣨtricyanic acid�����ų��w�⣬�ٲ���Ҳ����θ��������������D����5-������ण��M�����S��������ø��ȩ����ø���x������������ų��w�⡣
��������քe�δι�θ�o���漪�W�z�ң�S-1���̓������������/��ӷ�Ƭ��UFT�����ڽoˎ��0. 25��0. 5��1��2��4��8��12 ��24 h ��քe�y��Ѫ�{���[���M����5-FU�ĝ�ȼ���Ч�r�g��RNAˮƽ���[���M����������ϳ�ø���������õȡ�ԇ�Y���������漪�W�z�ң�S-1���oˎ�M��Ѫ�{���[���M���е�5-FU��Ⱥ���������e��AUC���քe��30μmol•h -1•L -1��95μmol •h -1•kg -1����UFT �oˎ�M��2. 0��1. 8�����漪�W�z�ң�S-1���oˎ�M���[���M����������ϳ�ø�������ʱ�UFT �oˎ�M��5 %��8 %��RNAƬ���Г���5-FU������UFT�oˎ�M��1. 6����
1. 3 ˎЧ�W
����ģ���@ʾ���漪�W�z�ң�S-1�����@��������ֲ�������w�ȵ����Y�c����θ�����^�i���������ٰ����������L��������Ч�������[���������D�ơ����ͬ�r�@ʾ���漪�W�z�ң�S-1���������θ�c���������^�p������Yoshida ��������У��漪�W�z�ң�S-1����ED50��5 mg•kg -1����AH-130��Sato �ΰ�����ģ���У��漪�W�z�ң�S-1���@ʾ����UFT ���õ�����Ч���������ѳ���ģ���У��o���漪�W�z�ң�S-1��20 mg•d -1�������[�����L�ķ����ʞ�89 %�����c��K��1 mg•kg -1������ˎ���������ʿ��_99 %��
Takechi�Ȍ��˷ΰ�������ֲ�������w�ȣ��քe�o���漪�W�z�ң�S-1����UFT��5-FU��5-�������Ó�����գ�5′-DFUR��14d���O�y�俹�[�����Լ��[��������������ऺ������ø��DPD���������Ó���������ữø��TP������������������D��ø���ԡ��Y���������漪�W�z�ң�S-1���������������@��������Nˎ��C�ͷ����Y���������漪�W�z�ң�S-1����UFT�������������ƣ���������ˎ������һ�M�������[��������4 �Nø�Ļ��ԣ��漪�W�z�ң�S-1��Ҳ�@ʾ���������������
1. 4 ����W
Hayashi �ȷքe�y���˴���С������漪�W�z�ң�S-1����CDHP��OXO�Ć΄������ԡ��Y����������1���漪�W�z�ң�S-1������Ҫ�����Þ鸹�a�����Ѻ�Óë�����ؕr����ɳ��F�w�p�p��˥�����l�Ի�Ӝp�١�ؚѪ�������t���ȰY���2�����ڷ��漪�W�z�ң�S-1���Ą����M�в���z��l�F�����ք�����F�β���Ѫ��ˮ�[�����cϵĤ�ܰͽY̎�а��tɫ���c�����ٺ��ܰͽY�ɳ��Fή�s��Ƣ�K���cϵĤ�ܰͽY���ܰͼ����p�٣����輚���p�٣�θ���w��Ѫ���ڷΡ��λ�Ƣ�г��F�����ۼ�����3���漪�W�z�ң�S-1����FT�ĺ���Ӌ��С�������LD50��Ӌֵ�քe��549��441��551��53 mg•kg -1����4�������ԣ��������ԣ���CDHP��OXO��LD50������2 000 mg•kg-1����5���漪�W�z�ң�S-1��������ԭ������c��Ѫϵ�y���ܰͽY�p�����Լ�����ϵ�y������ϵ�y�������P���漪�W�z�ң�S-1���Ķ��Է�ӳ��5-FU�Ķ��ԣ�����CDHP ��OXO֮��δ���F�������ԡ�
Kitajima�Ȍ������L�ڶ��Ԍ���@ʾ�������քe�ڷ��漪�W�z�ң�S-1��0��0. 004 ��0. 02 mg•kg -1•d-152�ܣ���ˎ���g���������F������������ͣˎ����ʧ���H�нYĤ��׃��Ƥ�wɫ�س�������Ĥ���ܻ֏͡�
����������ǰ�ںͳ��ڽoˎ���������漪�W�z�ң�S-1����OXO��̥��İl�������������á�OXO�ڴ��Դ���������ڽoˎ߀���Ԯa����̥�������»����á��ڴ�����õ�̥�������γ��ڡ����a�ںͲ����ڽoˎ���漪�W�z�ң�S-1����OXO�����a���������l���t�����»����á�CDHP����������Ќ�����]��Ӱ푡�
�w����ͻ׃����@ʾ���漪�W�z�ң�S-1���o��ͻ׃���ã�����Ⱦɫ�w���»����á�CDHP���w��]����ͻ׃����Ⱦɫ�w��׃���á��w��Ⱦɫ�w��׃�����OXO�@��ԣ����ڻ؏�ͻ׃�Ԍ���О���ԡ�
2 �R��ԇ��Y��
2. 1 �R��ˎ�������W
���ձ��M�еĢ����R��ԇ�������漪�W�z�ң�S-1�����x����Ѫ�Юa��5-FU�ij�Ч�r�g�����^�L�����˥�ڞ飨13. 1±3. 1��h��ƽ�������r�g�飨13. 2±1. 7��h���ڷ���Ҏ�������漪�W�z�ң�S-1������ˎ�������W�������1�ͱ�2��
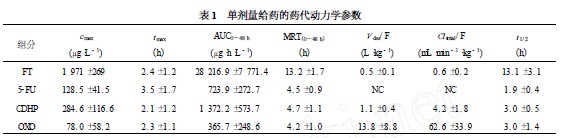
Cmax�����Ѫˎ��ȡ�tmax��Ѫˎ����_��r�g��AUC��Ѫˎ��ȕr�g��������e��MRT��ƽ�������r�g��Vdss��ˎ��ֲ��ݷe��Cltota��ȫ������ʡ� F�������ʡ�t1/2����˥�ڡ�NC������Ӌ�㡣
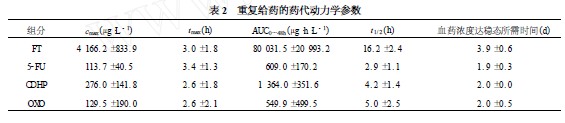
Chu���M�еĢ����R��ԇ��У�20�������[�����߷�3�������M�քe��50��60 ��70 mg•m-2•d-1��������72�����̣��B�m��ˎ4�ܣ�ͣˎ1�ܞ�1�����̣���ԇ�Y���@ʾ���漪�W�z�ң�S-1���Ą��������Բ��������鸹�����m���gʹ��ĸ��a��һЩ��ԇ�߿ɳ��F���ġ��I�¡�ճĤ��Ƥ����Y����^�p�������ܡ������R��ԇ�Y���@ʾ�������]������50 mg•m-2•d-1��
3. 2 ��ȫ�Լ���Ч
Sugimachi �����ձ��M������24���R��ԇ����Ĺ�ͬ���ӵ��u�r�漪�W�z�ң�S-1���ί�����θ���ͽYֱ�c���Ģ����R��ԇ31��θ�����ߺ�31���Yֱ�c���������xԓ��о���ÿ���������ٽoˎ2�����̣�ÿ�����̰��������߿ڷ��漪�W�z�ң�S-1�� 75��50 mg•m- 2•d - 1����FT Ӌ����ÿ��2 �Σ��B�m28 d���g��2 �ܺ����M����һ�����̡��Y���քe��28��θ�����ߺ�30���Yֱ�c�������u�r���漪�W�z�ң�S-1���į�Ч�Ͱ�ȫ�ԡ�ԇ��@ʾ��θ�����ߺͽYֱ�c�����ߵĿ���Ч�ʷքe��53. 6 %��15/28����16. 7 %��5/30����90 %���Ņ^�g�քe��38. 4 %��68. 1 %��8. 4 %��30. 5 %�����r�g��λ���քe��298 ��358 d��
Sakata ����һ���51 ������θ�����߅��ӵ��_����ԇ��У������漪�W�z�ң�S-1���Ŀ��[�����úͲ��������������ڷ��漪�W�z�ң�S-1��80 mg•m-2•d-1��ÿ��2�Σ�ÿһ�����B�m��ˎ28 d���g��14 d���؏���ˎ4�����̡�����1��������ȫ���⣬24�����־��⣬����Ч�ʞ�49 %�����������l���ʞ�78 %�����Ȳ��������l���ʞ�20 %������Ѫ�����p�١������p�ٰY�������������p�١����a��Ƥ�������δ�^�쵽���صIJ���������
Osugi �ȿ������漪�W�z�ң�S-1���ڸ�Ĥ�Uɢ��θ�������еį�Ч��ԇ���^��18�������漪�W�z�ң�S-1����80 mg•m-2•d-1��ÿ��2 �Σ��B�m28 d ��һ�����̣�ͣˎ14 d ���؏��@һ���̣���11���ڷ�5-FU�M�л����Ļ��ߴ���ڡ��Y���������漪�W�z�ң�S-1���M��5-FU�M���ߵ�ƽ���ɻ�r�g�քe��257 ��118d����ˣ������Ɯy�漪�W�z�ң�S-1������Ч���L��Ĥ�Uɢ��θ�����ߵĴ���ڣ����ƻ��ߵĺ��ڰY�
Kinoshita �Ȉ���˲����漪�W�z�ң�S-1����35 ��θ�������M��8�����̵��g���o���Ի����������������漪�W�z�ң�S-1��80��120 mg•kg-1•d-1���B�m��ˎ4 �ܺ�ͣˎ2�ܞ�һ�����̡��Y����������1����7���������[���Ͱl���˳�ԇ��������δ�Ͱl����4��������ʳ���p�˶�δ���ȫ�����̣�17�����ߣ�60. 7 %���Գ���ˎ8�����̣���2���딵���ϻ��������F�����������p�ٰY�������p�ٰY����đ�t�����ߡ�ʳ���p�ˡ�ƣ���o�������a�����ćI�¼���ǻ�Ȳ������������Т�������������p�ٰY�l���ʞ�29. 3 %�������p�ٰY�l���ʞ�9. 8 %�����a�l���ʞ�9. 8 %��δ���F���Ȳ���������
Maehara��B�˽��ڵăɂ������R��ԇ�Y�����漪�W�z�ң�S-1���Ŀ������ʞ�44. 6 %��45/ 101������λ���r�g��244d��1�������ʞ�37 %��
һ헢����R��ԇ�Y���@ʾ��Ч�^�á�Iwase�Ȍ�42��θ�������M���漪�W�z�ң�S-1��+ CDDP �ϻ����������漪�W�z�ң�S-1���ڷ�80 mg•m-2���B�m��ˎ14 d��ͣˎ14 d����1�����̣�����ˎ��8�죬�oעCDDP 70 mg•m-2���Y���@ʾ�������ʞ�50 %��������ȫ�����ʞ�5 %����λ����r�g��342d��2�����ʞ�22..9 %����7����16. 6 %�����߳��F��Ȳ���������2�����ߣ�22. 9 %�����F��Ȳ�����������ˣ��J���漪�W�z�ң�S-1����CDDP�ί�θ��Ч���^�á�
�ĬF�е��R�������������漪�W�z�ң�S-1����θ����Ч�^��ͻ������ˎ�ί�θ���������ʞ�35 %��55 %�����ٰ���Ч�ʼs40 %���Yֱ�c���s35 %���c��K���ί�θ����Ч�ʞ�25 %��60 %���cĿǰ�R����ʹ�õ�ˎ����ȣ������^�����@����Ҫ����������������ƺ�θ�c�����������а����p�ٰl����45. 8 %��Ѫ�t���לp�ٰl����37. 0 %�������������p�ٰl����44. 0 %��ѪС��p�ٰl����10. 5 %��ʳ������l����32. 7 %�����ġ��I�°l����26. 8 %�����a�l����17. 4 %����ǻ�װl����15. 7 %��ɫ�س����l����20. 0 %��Ƥ��l����10. 9 %���̶�һ���^��غ͡�Ŀǰ�����겻�H���ɇ���ɽ�|�r��ˎ�I��˾���a���漪�W�z�ң���Ʒ�����S���_�������N�ۣ������ڽ����°����ձ����iˎ�I���a���漪�W�z�ң���Ʒ������˹�f��Ҳ�ѽ����Ї����С�����漪�W�z�������ɞ�θ��������һ����ˎ��
TAG���漪�W�z�� S-1 θ�� �S���_ ��˹�f
���PˎƷ

�������- ��Ҋ���} | ����ָ�� | ˎ�W���� | ���Ҋ | �Ͷ�V | ���Ʒ��� | ���t��ˎ | ˎ������
���Ʒ����- �[���� | �β��� | �� | ����� | Ƥ�w�Բ��� | �� �� | �L�����߿� | ��Ѫ�ܿ� | ���� | ��������ˎ
ˎƷ����- �[����ˎƷ | �����ˎƷ | �β���ˎƷ | �ۿ�ˎƷ |Ƥ�w�Բ���ˎƷ | ��ˎƷ | �L�����߿�ˎƷ
�ٝ�ˎ���Y�|- ��I���ˠI�I���� | ���WˎƷ��Ϣ�����Y���C







