���F�ڵ�λ�ã� �ٝ�����ˎ���W��� >> �[���� >> �[����Ҏ��ˎ�����
�������I(ϣ�_�_)+�Wɳ���K�����ڽY�c���ί��˜�
- ��Դ�� �Ї��t�WՓ���� ���ߣ�����܊ �g�[�� �l���r�g��2009/11/19 8:46:00
���ÚW�����Y����ߚW���[���ȿƌW����ECCO15-ESMO34�����������NO16968��XELOXA���������I��ϣ�_�_�����Wɳ���K�ݣ��о��Y���@ʾ���c��Ҏ�o�}ע�仯��ˎ��5- �������/���~�ᣨ5-FU/LV����ȣ�XELOX�ۿ������I��ϣ�_�_�����Wɳ���K���@�����L���ߟo�������ڣ��ί��Y�c������Ч�����ɞ����ڽY�c���o���ί����˜ʡ�
�ڱ���ECCO/ESMO����ϣ������R���t���Pע�ć��H�� ��NO16968 �о���XELOXA�ۿ������I��ϣ�_�_�����Wɳ���K�ݣ������½Y��������ƽ���S�L57���µĽY���@ʾ���c��Ҏ�o�}ע�仯��ˎ��5-FU/LV��FOLFOX ��������ȣ��g��ڷ��������I��ϣ�_�_�����o�}��ע�Wɳ���K����XELOX�������ί������@�����L���ڽY�c�����ߵğo�������ڣ���������Ҳ�@�F������څ�ݡ�
NO16968 �о��Y���C�����ڽY�c���o�������I��XELOX�ۿ������I��ϣ�_�_�����Wɳ���K�� ��������˜�FOLFOX ������������ɞ�Y�c���µĘ˜��ί�������
�ښW�ޣ��Yֱ�c���ǵڶ���Ҋ�[������ԭ����ȫ���ǵ�����Ҋ�[����ȫ��ÿ��s�_�\100 �f���°l�Yֱ�c�������о��Y���Ĺ������o�ɞ�Y�c�����ߎ����˸�����ʹ��������һ������Ч������ȫ���������ί��x��
NO16968�����
NO16968 �о���XELOXA����һ��u�r�ڷ��������I��ϣ�_�_�����o�}��ע�Wɳ���K��XELOX���c5-FU/LV ������ڽY�c�������g���o���ί���Ч���_���ԡ��S�C���� ���R���о���
��2002 ��Ӌ����헱��о��r���oՓ��÷�W��Mayo��߀���_Ɲ�f�����ˣ�Roswell Park���������Y�c���Ę˜��o�����������o�}ע��5-FU/LV�����r�����ڱ��^�������I��ϣ�_�_���cMayo�����ڢ��ڿ��г��Y�c���o���ί������õĢ����R���S�Cԇ�——X-ACT �о��ij����Y���C�����������I��ϣ�_�_���ί����ڽY�c�������c5-FU/LV ��Ч������^����5-FU/LV ���A���ϊWɳ���K�ί����ڽYֱ�c���Ĵ����о���NSABP C-07 ��MOSAIC��Ҳ�����M��֮�С�
�����^��ڷ��������ϊWɳ���K�ί����ڽY�c���į�Ч������X-ACT �о��Y�����о����x���˿������I��ϣ�_�_���c�Wɳ���K���ί��c�˜ʷ���(�oע5-FU/LV) �M�б��^��NO16968��XELOXA �о�����XELOXA�ۿ������I��ϣ�_�_�����Wɳ���K�� �о�Ҳ��˳ɞ��cNSABP C-07 ��MOSAIC ͬ�r�M�еġ���3 ��^��Wɳ���K�ڽY�c���o���ί������õ��о����cNSABP C-07 �о���MOSAIC �о����{���ˢ� �ں͢� �ڽY�c�����ߣ���ͬ���ǣ�XELOXA�ۿ������I��ϣ�_�_�����Wɳ���K���о��H�{���ˢ��ڽY�c�����ߡ�
NO16968�о��OӋ
NO16968 �о����{��1886 ���� �ڽY�c�����ߣ���29 �����ҵ�226 ���о�����ͬ�r�_չ���Ї�����11 �����ą��ӡ�ԓ�о�����Ҫ�K�c���^��XELOX �ۿ������I��ϣ�_�_�����Wɳ���K�ݷ��������L���ߟo�������ڣ�DFS�������Ƿ���5-FU/LV����Ҫ�K�c�������������ڣ�OS������ȫ�Ժͷ�ˎ�����Ե��u�r��
�ί�������944 ������XELOX �������������I1000 mg/m2��2 ��/�գ�d1-14���Wɳ���K130 mg/m2 d1��ÿ3 ��1 �Σ�8���ڣ��ί���942 �������oע5-FU/LV �ί���Mayo ����n=664�� Roswell Park ����n=278�������ί�6 ���¡�
NO16968��Y��
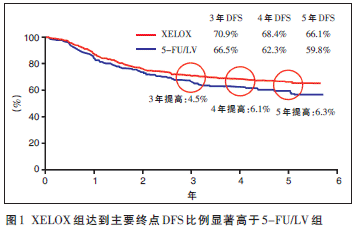
�о��_������Ҫ�K�c��ƽ���S�L57���µ������ί���ITT����Ⱥ�����Y���@ʾ��XELOX�ۿ������I��ϣ�_�_�����Wɳ���K���ί��M�_����Ҫ�K�cDFS�����@������5-FU/LV�ί��M[Σ�U�ȣ�HR��=0.80��95%���Ņ^�g��CI����0.69~0.93��P=0.0045]������3��DFS���4.5%��4��DFS���6.1%��5��DFS�����6.3%���D1�����@�������S���r�g�����L�����ߵ�������u���ӡ�
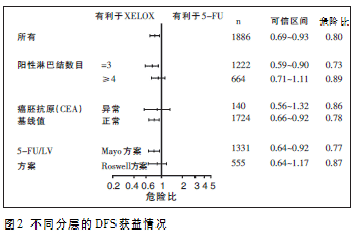
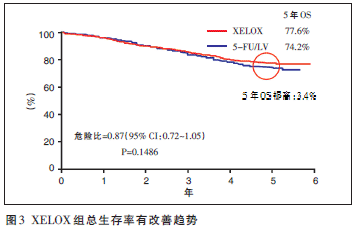
��ͬ�ӵ�DFS�Y���@ʾ���c�ܰͽY������4�Ļ�����ȣ��ܰͽY������3�Ļ����ί��@����ã��D2����XELOX�ۿ������I��ϣ�_�_�����Wɳ���K���ί��M�Ĵ�Ҫ�K�c�������ʣ�OS���и��Ƶ�څ�ݣ�5��OS�����3.4%��HR=0.87��95%CI��0.72~1.05��P=0.1486���D3�����Mһ���ĽY�������S�L�С�
�S���S�L�r�g�����L��XELOX�ۿ������I��ϣ�_�_�����Wɳ���K�ݽM�ī@����ܕ���u׃���@�������@���棬MOSAICԇ���Խo�҂�һЩ��ʾ����MOSAICԇ��OS����������FOLFOX-4������OS�@������u�@�F�ģ��������S�L5���FOLFOX-4������5-FU/LV������OS�@�淽������u����ʹ��FOLFOX-4�����Ļ��ߵ�6�꿂��������@������ʹ��5-FU/LV�����Ļ��ߡ�����MOSAICԇ����λ�S�L�r�gĿǰ�ѽ��_81.9���£���NO16968ԇ�Ŀǰ����λ�S�L�r�gֻ��57.1���£�����S���S�L�r�g�����L��NO16968ԇ���XELOX�ۿ������I��ϣ�_�_�����Wɳ���K�ݽM���߳��F�@����OS�@����ֵ���ڴ��ġ�
���⣬�����зǰ��Y���P������XELOX�ۿ������I��ϣ�_�_�����Wɳ���K�ݽM�ğo�Ͱl�����ʣ�RFS��Ҳ�@����ߣ�HR=0.78��95%CI��0.67~0.92��P=0.0024��������3��RFS���4.6%��XELOX�M��72.1%��5-FU/LV�M��67.5%����4��RFS���6.4%��XELOX�M��69.7%��5-FU/LV�M��63.3%����5��RFS�����6.9%��XELOX�M��67.8%��5-FU/LV�M��60.9%����
�c5-FU/LV�ί���ȣ�XELOX�ۿ������I��ϣ�_�_�����Wɳ���K���ί��@ʾ�����õİ�ȫ�Ժ������ԣ������Ǵ���˹������ƵĶ��Է�����������C�����l���������ǿ���ͨ�^�{�������͌��Y�ί������Ƶġ�
NO16968������x
�L���ԁ�������Y�c���Ę˜ʷ�����FOLFOX�����V���������R���������}Ҳ������������ȣ��o�}���m��ע5-FU��������o�}�ף����������o�}���ܣ�PICC���mȻ���Ա��⻯����ɵ��o�}�p�������ùܵIJ�����L�UҲ��Ӱ푻���������M�С����⣬FOLFOX�����е�5-FU��Ҫ�����ó��m��ע�Լ�ÿ2��1�ε�סԺ�ί����Ȏ����˲��㣬���������M�ã���˺ܶ�߲��܈Գ�6����12���ڵĘ˜�FOLFOX�����������Ķ�Ӱ��˯�Ч��
X-ACT ԇ��C�����ڽY�c���g���o�������У��������I�����5-FU�����������P�ĵ��ǣ��������I��ϣ�_�_���ϊWɳ���K��XELOX �����Ƿ���Ԍ�FOLFOX �Ľ�˜�������𡣴˴�ECCO/ ESMO����Ϲ�������Ҫ�о�——NO16968��XELOXA�ۿ������I��ϣ�_�_�����Wɳ���K�ݣ��ش����@һ���}���������I��ϣ�_�_���ϊWɳ���K�o���ί��į�Ч�cFOLFOXһ�£����ҿɎ������õİ�ȫ�ԡ��@һ�Y����XELOX�ۿ������I��ϣ�_�_�����Wɳ���K�� �����ɞ��µĽY�c���o�������˜ʷ����ṩ�ˏ��������C����
���������о��Y�����������I��ϣ�_�_���ϊWɳ���K���������������ڽY�c�������o���ί��µĘ˜ʷ�����
TAG���������I ϣ�_�_ �Y�c�� XELOX
���PˎƷ

�������- ��Ҋ���} | ����ָ�� | ˎ�W���� | ���Ҋ | �Ͷ�V | ���Ʒ��� | ���t��ˎ | ˎ������
���Ʒ����- �[���� | �β��� | �� | ����� | Ƥ�w�Բ��� | �� �� | �L�����߿� | ��Ѫ�ܿ� | ���� | ��������ˎ
ˎƷ����- �[����ˎƷ | �����ˎƷ | �β���ˎƷ | �ۿ�ˎƷ |Ƥ�w�Բ���ˎƷ | ��ˎƷ | �L�����߿�ˎƷ
�ٝ�ˎ���Y�|- ��I���ˠI�I���� | ���WˎƷ��Ϣ�����Y���C







