�༪�����} >> �༪���ί��I����II���R���о�
�༪���ί��I����II���R���о�
- ��Դ�� �ٝ�����ˎ���W �l���r�g��2007-3-13 15:32:00
���ڵ��R��II���о�Ӌ������һ헴��ڵķ��B�m���S�C���о����о�100391�����@��о������Ҫ���x�Yֱ�c�����ߣ�ͬ�r��M�������ڌ��w�����ߡ��ڳ����Y���@ʾ�����I��������Ч���@��о�����Ҫ�о�Ŀ���������I��������Ҳ�M�����S��ᘌ������[�����R��II���о����l�FijЩ���ܮa��Ч�����ض����N��
�о��п�Ӌ��M501�����N�����[������,������202������RCC����,32������δ�����^�κ��ί����@32����������һ���ί�������RCC����,�o�Mչ������50%,�o�Mչ����r�g��140��
��ˎ�о�
������II���о��l�F��Sorafenib��ˎ�ί����܌�ijЩ�[���R����Ч�ľ���������Mһ���M����2�II���о����о�100391��10874�������Y���£�Ҋ��5-2�����о�100391��һ헷��B�m���S�C�о������Ѕ������Ƚ��^12�ܵ��T���ڣ����o��Sorafenib 400mgÿ�Ճɴοڷ���12�ܺ����ٱ��F���p�Ⱦ���Ļ����^�m�o��Sorafenib�ί��������Mչ�Ļ���ֹͣ��ˎ�����������Ļ������S�C���밲ο���M��Sorafenib�M�M���ί������о���������˸��N���ڌ��w���������OӋ�r��Ҫᘌ��Yֱ�c�������Uչ���I���������[����͡��о�10874���ί��μ����ΰ����_���Էnj����о�����5-2�г����ѽY���Ć�ˎII���о���
��5-2���ѽY����Sorafenib��ˎII���о�
|
�о���̖ |
���Ӈ��� |
�[����� |
��ȫ���u�r��Ч������ |
|
100391 |
������Ӣ�� |
�����y���Ԍ��w��
����Ҫ��Yֱ�c�����I���� |
501 |
|
10874 |
�����r����������ɫ�С������������ |
�μ����ΰ� |
137 |
��ֹ��2004��12��31�գ�߀��4�Sorafenib��ˎII���о������M���У������о�11515��100555��100557��10941�����о�11515�����ձ��M�еĆ�ˎ�ί��I����II���о�����ֹ��2004��12��31�գ���2��������M���о�100555��һ��ί��D�������ٰ��Ķ�����������������_�����о�������54�����߽����ί����о�100557��һ��������͵��M�е��ί���С�����ΰ���II���о�����ֹ��2004��12��31�գ�����52��������M���о�10941���������ͷ����M�е�һ��ί�������������Ѫ����CML����II���о�����ֹ��2004��12��31�չ���10�����߽����ί�����5-3�г��������M�еĆ�ˎII���о���
��5-3���M���е�Sorafenib��ˎ�ί���II���о�
|
�о���̖ |
���Ӈ��� |
�[����� |
�ί�����������ֹ��2004��12��31�գ� |
|
11515 |
�ձ� |
�I�� |
2 |
|
100555 |
����������������� |
���ٰ� |
54 |
|
100557 |
�������� |
��С�����ΰ� |
52 |
|
10941 |
���������� |
������������Ѫ�� |
10 |
�о�100391
�о�100391�ĽY���Mһ���C����Sorafenib���ί������I��������Ч���о�100391�е���Ҫ��Чָ���ǻ����S�C�ֽM12�ܺ�ğo�Mչ�����ʣ���ָ�S�C�ֽM��12+3�܃ȼ���������Ļ���ռ����M���ߵİٷֱȡ���������S�C�ֽM��15��δ�M���[���u�����t����һ���[���u���ĽY����ʡ��������һֱδ�M���[���u���Ļ��߄t�J�����[���Mչ����5-10���Y���S�C�ֽM��12�ܵğo�Mչ�����ʡ�
��5-10���о�100391���I�������S�C�ֽM��12�ܟo�Mչ������r���Y
��������Ⱥ�����Ѕ����S�C�ֽM���I�����ߣ�
|
�yӋ�Wָ�� |
Sorafenib�M����32���� |
����M����33���� |
|
�o�Mչ�����˔� |
16 |
6 |
|
�o�Mչ�����ʣ�%�� |
50.0 |
18.2 |
|
95%���Ņ^�g��%�� |
31.9-68.1 |
7.0-35.5 |
|
Pֵ |
0.0077 | |
�S�C�ֽM12�ܺքe��50%��Sorafenib�M���ߣ�16/32����18%�İ�ο���M���ߣ�6/33�������o�Mչ���ɽM���^�Y���нyӋ�W���P=0.0077����
28����ο���M���߳��F�����Mչ����λ�����Mչ�r�g��7�ܣ���Ğ����Sorafenib�ί����@Щ���߸Ğ�Sorafenib�ί������Y���ί�����λ�r�g��24�ܣ������ڸ���Sorafenib�ί�������_ʼ�Mչ�����µõ����ơ�
�о���߀�����˟o�Mչ����r�g���S�C�ֽM��ο���M���ߵğo�Mչ����r�g��41�죬Sorafenib�M���ߵğo�Mչ����r�g��163�죬�ɽM���^�нyӋ�W���P=0.0001�����ί��M���ߵğo�Mչ����Kaplan-Meier����Ҋ�D5-5��
�D5-5���о�100391����M�I�����ߵğo�Mչ���棨�죩Kaplan-Meier����
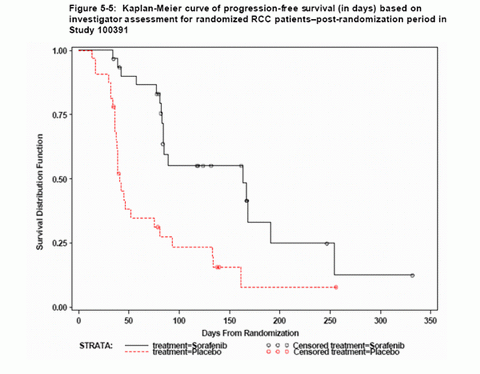

�������I�����ߣ��������Ӻ�δ�����S�C�ֽM�ߣ��ğo�Mչ�����M�з��������о����ж�����λ�o�Mչ����r�g��162�죨95%���Ņ^�g��137-183�죩�������������ҽM�����C���ğo�Mչ����r�g��140�� ��95%���Ņ^�g��123-161�죩��
TAG�� �༪�� �I�� �ΰ�
���PˎƷ
���ˎ�v��ۙ

ʮ��ȫ���B�i����ˎ����ȫ���Ҍ����B�iˎ�������wȫ���^���Д�ʮλ�̘Iˎ����
�ٝ������̳ǡ����WˎƷ�������Y���C���� ��C20110003

- ���Ʋ��N������
- �[����
- ���
- ��
- �����
- Ƥ�w�Բ���
- �ۿ�
- �L�����߿�
- ���XѪ�ܿ�
- ����
- ������ֳ��
- �I�B������
- �t�����
- ˎƷ�f����������
- �[����
- ���
- ��
- �����
- Ƥ�w�Բ���
- �ۿ�
- �L�����߿�
- ���XѪ�ܿ�
- ����
- ������ֳ��
- �I�B������
- �t�����
- �ټ{���쯏��|������ˮ�ͣ�
- �ڣ�Ҹ��̽�w��Ӌ
- �Wķ���ϱ�ʽ���Ѫ��Ӌ HEM-1000
- ��ȫ�Ԅӱ�ʽ���Ѫ��ӋHL-888QA
- ��������������Ѫ�ǃx���yɫ��
- YX300��ָ�Aʽ�}��Ѫ���x
- ��������������Ѫ�ǃx����ɫ��
- �~�S�Ԅ��_�PѪ��Ӌ
- ؐ��EZԇ��25S
- �~�S������YU730
- ؐ��EZѪ�ǃx
- MiKi��ɫ����ʽ������MWS-S66-010-041
- �~�S��ʽ���Ѫ��ӋYE8700A
- ����ȫ�Ԅӱ�ʽ���Ѫ��ӋDB-31
- �~�S����ͨ�õ��_860
- ӯ�ز��P䓿������ʣ�ע�ܰ�)IT702
- �~�SH020B������
- �����Σ����ۯB��FS899
- ���Z����Ѫ�ǃx��50S
- ����˹������֬�z��
- ��������������Ѫ�ǃx���tɫ��
- �~�S����YU831
- MiKi݆��܇MPT-43L����̥
- ӯ�ػ�ӷ��և���������IT806
- �Wķ���ϱ�ʽ���Ѫ��Ӌ HEM-746C
- ����
- ˎƷ���}������
- A
- B
- C
- D
- E
- F
- G
- H
- I
- J
- K
- L
- M
- N
- O
- P
- Q
- R
- S
- T
- U
- V
- W
- X
- Y
- Z
- ���oӛ�
- ���oӛ�
- ���oӛ�
- ���oӛ�
�Wվ�YӍ- ˎ����B |
�B�i�T��ֲ� | �˲���Ƹ |
ϵ�҂� | �Wվ�؈D
�������- ��Ҋ���} | ����ָ�� | ˎ�W���� | ���Ҋ | �Ͷ�V | ���Ʒ��� | ���t��ˎ | ˎ������
���Ʒ����- �[���� | �β��� | �� | ����� | Ƥ�w�Բ��� | �� �� | �L�����߿� | ��Ѫ�ܿ� | ���� | ��������ˎ
ˎƷ��ُ����- �[����ˎƷ | �����ˎƷ | �β���ˎƷ | �ۿ�ˎƷ |Ƥ�w�Բ���ˎƷ | ��ˎƷ | �L�����߿�ˎƷ
ˎ���Y�|- ��I���ˠI�I���� | ˎƷ���I�S���C | ˎƷ���I�|������Ҏ���J�C | ʳƷ�l���S���C | ���WˎƷ��Ϣ�����Y���C
�������- ��Ҋ���} | ����ָ�� | ˎ�W���� | ���Ҋ | �Ͷ�V | ���Ʒ��� | ���t��ˎ | ˎ������
���Ʒ����- �[���� | �β��� | �� | ����� | Ƥ�w�Բ��� | �� �� | �L�����߿� | ��Ѫ�ܿ� | ���� | ��������ˎ
ˎƷ��ُ����- �[����ˎƷ | �����ˎƷ | �β���ˎƷ | �ۿ�ˎƷ |Ƥ�w�Բ���ˎƷ | ��ˎƷ | �L�����߿�ˎƷ
ˎ���Y�|- ��I���ˠI�I���� | ˎƷ���I�S���C | ˎƷ���I�|������Ҏ���J�C | ʳƷ�l���S���C | ���WˎƷ��Ϣ�����Y���C







